线粒体自噬是为了维持细胞稳态,细胞通过选择性地清除多余的、或者功能受损的线粒体,以维持线粒体数目和质量的平衡:多余的或者损伤的线粒体会被特异性的包裹进自噬体中并与溶酶体融合,从而完成线粒体的降解。
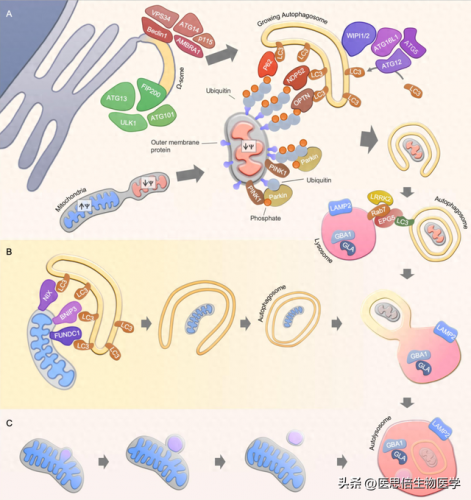
(A)泛素依赖性PINK1-Parkin介导的线粒体自噬
线粒体损伤后,PINK1在线粒体外膜处稳定,导致Parkin活化和随后线粒体蛋白的泛素化。招募自噬受体如NDP52,OPTN和p62,通过与LC3的相互作用介导自噬体膜对线粒体的吞噬。自噬体膜的可以由内质网提供,其中自噬核心复合物VPS34和ULK1启动膜形成。膜形成进一步由WIPI1和WIPI2介导,导致ATG16L1复合物和LC3的募集,从而促进自噬体的形成。最后,自噬体与酸性溶酶体融合,这一步骤由自噬体和溶酶体蛋白的协同作用调节。
(B)泛素非依赖性受体介导的线粒体自噬
泛素非依赖性受体介导的线粒体自噬是由自噬受体蛋白(如 NIX、BNIP3 和 FUNDC1)富集到线粒体膜,募集LC3并与之结合,使自噬体吞噬线粒体。
(C)替代降解途径
零碎的线粒体自噬和线粒体衍生的囊泡降解是介导线粒体局部降解的细胞途径。
今天给大家分享一篇发表在Journal of translational medicine期刊题为“Protective effects of Gypenoside XVII against cerebral ischemia/reperfusion injury via SIRT1-FOXO3A- and Hif1a-BNIP3-mediated mitochondrial autophagy”的研究论文。

研究背景
线粒体自噬在脑缺血再灌注损伤的病理过程中起着重要的作用。对于环磷酰胺十七(gp17)是否对线粒体自噬有调节作用尚不清楚。先前的研究发现,GP17可以显著抑制认知损伤并减轻MPTP和谷氨酸诱导的神经元氧化损伤,表明GP17具有神经保护作用。GP17可以通过抑制内皮细胞凋亡、氧化应激和内质网应激诱导的线粒体损伤来发挥药理作用。还可以增强溶酶体生物合成并通过TFEB激活加速淀粉样蛋白B的自噬清除。GP17在缺血性脑损伤中谓节自噬的神经保护作用尚未研究,也不清楚GP17和三七皂的活性成分是否通Hif-1ɑ/BNIP3途径调节自噬。
本文的研究目的是探讨GP17在改善缺血性中风的神经保护作用及其调节自噬的分子机制。通过研究GP17对线粒体损伤和缺血诱导的神经细胞凋亡的影响,以及GP17对自噬相关蛋白的调节作用,揭示GP17的神经保护机制,并为开发治疗缺血性中风的新型药物提供理论依据。
研究思路
本文主要通过动物实验和细胞实验,研究了GP17对缺血再灌注损伤的神经保护作用,并探究了其调节线粒体自噬相关通路的机制。利用动物手术、药物处理、行为评估、组织染色、蛋白表达检测、细胞模型构建、细胞功能检测等实验方法,揭示了GP17通过调节线粒体自噬通路发挥神经保护作用的机制。
主要研究成果
1. GP17对缺血性中风具有预防和治疗效果。
2. GP17具有神经保护作用,可以减轻急性脑缺血引起的病理变化、氧化损伤和炎症反应。
3. GP17通过调节线粒体自噬途径发挥神经保护作用。
4. GP17通过NAMPT-SIRT1途径调节Hif1a-BNIP3通路,发挥神经保护作用。
5. GP17可以调节自相关蛋白的表达,激活线粒体自噬途径。
研究结果
1. GP17 可减轻缺血大鼠脑梗死,改善神经功能缺损评分,减轻神经元病理损伤
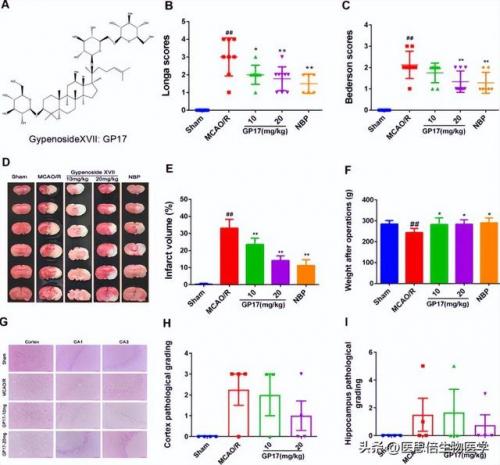
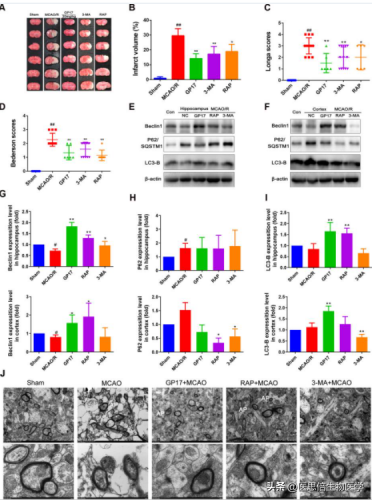
在 MCAO/R 大鼠的治疗效果研究中,10mg/kg、20 mg/kg 的GP17 预处理显著降低缺血后 24 h 的 Longa 评分和Bederson 评分(图 1B, C)。在缺血前 7 天,10mg/kg、20 mg/kg 的 GP17 显著减少梗死体积(图 1D, E)。GP17 (20mg/kg)处理的大鼠表现出与 dl-3-正丁基苯酞(NBP)处理的大鼠相似的神经功能缺损评分。因此,与 MCAO/R大鼠相比,gp17 处理的大鼠的体重恢复更好(图 1F)。在20 mg/ kg 的剂量下,GP17 也减少了皮质区(图 1G, H)和海马区(图 1G, I)核固缩的发生。此外,GP17 (20 mg/kg)预处理显著降低了炎症细胞因子 IL-6、TNF-α 和 MCP-1 以及氧化细胞因子 T-AOC 和4-HNE 的表达水平(附加图 S1A-E)。
2. GP17在体内通过调节线粒体自噬来预防CIRI
为探讨急性缺血模型对线粒体自噬功能的调节作用,缺血前7天在腹膜内注射雷帕霉素、自噬诱导剂和自噬抑制剂3-MA。有趣的是,RAP(200µM)和 3-MA (2 mM)均显著减少梗死体积(图 2A、B)和神经功能缺损评分(图2C、D)。此外,GP17 对梗死体积和神经功能缺损评分的影响强于 3-MA 和 RAP。WB结果证实,在海马和/或 皮 层 组 织中,GP17、RAP 和/或 3-MA 增 加 了Beclin1 和 LC3-B 的表达,抑制了 P62 的表达(图 2E-I)。透射电镜(TEM)结果显示 MCAO/R 诱导了自噬小体的积累,而 GP-17、RAP 和 3-MA 处理促进了多个自噬空泡的形成(图2J)。
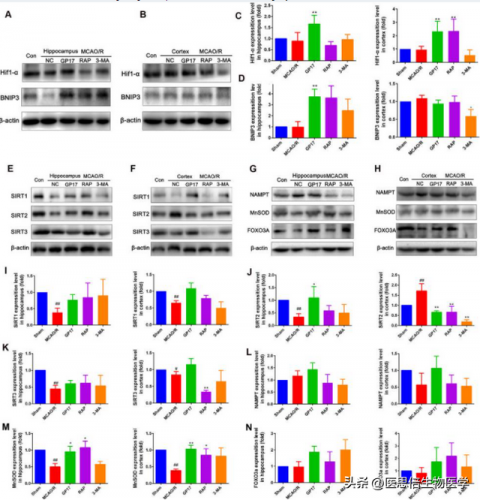
3. GP17通过激活Hif1α-BNIP3和SIRT1/2-FOXO3A信号通路调控大鼠缺血后线粒体自噬
作者想知道Hif1α 和 BNIP3 是否参 与了 GP17 调控自噬的机制 。WB 结果显示,与 MCAO/R 大鼠相比,GP17预处理显著提高了海马和/或皮质组织中 Hif1α 和BNIP3 的表达。此外,RAP 预处理可激活皮质内的Hif1α 和海马内的 BNIP3。与 MCAO/R 单独作用的大鼠相 比,3-MA(抑制剂)处理的大鼠海 马和皮 质 区中 Hif1α 和BNIP3 的表达没有显著差异(图 3A-D)。
作者前期研究发现,NAMPT-SIRT 通路可增加神经元的缺血耐受性,抑制神经元凋亡和坏死,改善缺血下的能量代谢。在本研究中,作者发现与假手术大鼠相比,缺血大鼠海马和/或皮层中 SIRT1/2/3 的表达显著激活,但GP17预处理明显减弱缺血大鼠缺血后SIRT1/2表达的变化(图 3E-F, I-K)。为了进一步探讨 GP17 对 NAMPT- sirt1 /2 调控的下游蛋 白 的 影 响 , 我 们 检 测 了 NAMPT 、 FOXO3A 和MnSOD 的表达,并探讨了 GP17 对 FOXO3A 的调控作用。我们发现,与对照组相比,用 GP17 处理的大鼠海马区和/或皮质区 NAMPT、MnSOD 和 FOXO3A的表达更高(图 3G-H, L-N)。提示 GP17 通过 NAMPT激活下游 SIRT1/2 蛋 白的表达,上调 FOXO3A 和MnSOD 的表达,抑制线粒体氧化损伤,改善能量代谢,从而抑制缺血引起的神经损伤。
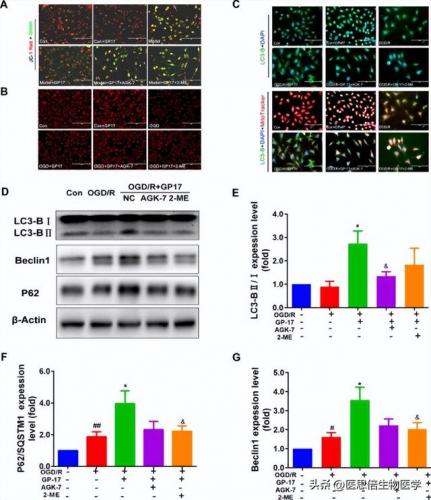
4. GP17通过调节线粒体的体外自噬作用来减轻OGD/R诱导的 SH - SY5Y细胞损伤
为了更好地表征 GP17 对线粒体自噬调节的作用,并确定其可能的机制,作者首先在体外检测了 OGD/ r 作用下 的 SH-SY5Y 细 胞 的 自 噬 泡 。GP17 显 著 增 加 了OGD/R 诱导形成的酸性自噬小泡的数量和荧光强度。为了探讨自噬是否参与了 GP17 对 OGD/ r 诱导的 SH-SY5Y 细胞损伤的影响,在对 OGD/ r 诱导的 SH-SY5Y细胞进行 RAP 和 3-MA 处理的同时,对 GP17 进行处理。结果表明,RAP 预处理进一步增加了酸性自噬小泡的数量和荧光强度,而 3-MA 几乎完全消除了 GP17引起的酸性自噬小泡数量和荧光强度的增强(图 4A)。为了在体外检测自噬溶酶体,我们用 GP17 孵育 OGD/r 作 用 的 SH-SY5Y 细 胞 , 并 用 Lyso-Tracker Red 和MitoTracker Green 免疫染色检测自噬溶酶体。在 OGD/ r 作用下的 SH-SY5Y 细胞中,GP17 显著增加了自噬(4B)。根据自噬标记物 LC3-B(绿色)和线粒体标记物 MitoTracker Red 的共定位来评估线粒体吞噬体的形成(4C)。作者继续检测 SH-SY5Y 细胞中主要线粒体自噬信号通路相关蛋白的表达,发现在 OGD/ r 作用的 SH-SY5Y 细胞中,GP17 增加了 LC3-B 和 Beclin1 的表达,p62 的表达被抑制。RAP 加速了除 p62 外所有蛋白的上调(图 4D-G)。

5. SIRT1/2 和 Hif1α 抑制消除了 GP17 对 OGD/ R 作用的 sh - SY5Y细胞中线粒体自噬相关指标的影响
为了评估 SIRT1/2 和/或 Hif1α 信号通路是否与 GP17 的线粒体自噬相关指标相关,作者使用 SIRT1/2/3 抑制剂AGK-7 和 Hif1α 抑制剂 2-ME 与 GP17 一起治疗 SH-SY5Y 细 胞 。首 先 , 作者研 究 了 AGK-7(0.1、0.5、1.0、5.0 和 10µM)和 2-ME(1.0、5.0、10.0和 20.0µM)处理的正常 SH-SY5Y 细胞的活力。作者选择 0.1µM AGK-7 和 2.5µM 2-ME 进一步验证 GP17 调控线粒体自噬的分子机制。接下来,评估了 OGD/R 和 GP17 或 AGK-7 和 2-ME 处理后 SH-SY5Y 细胞的线粒体膜电位(MMP)和活力。AGK-7 或 2-ME 均降低了 GP17-和OGD/ r 共处理的 SH-SY5Y 细胞的 MMP 和线粒体活力(5A、B),为了确定 GP17 对线粒体功能的影响,作者在海马实验中分别通过测量氧消耗率(OCR)和细胞外酸化率(ECAR)来评估氧化磷酸化和糖酵解作用。AGK-7 和 2-ME 均显著抑制 GP17 增强的 GFP-LC3-B和 MitoTracker Red 的共定位(5D)。WB结果也证实AGK-7 和/或 2-ME 降低了 GP17 和 OGD/R 共处理组LC3-B、Beclin1 和 p62 的表达(图 5E-G)。
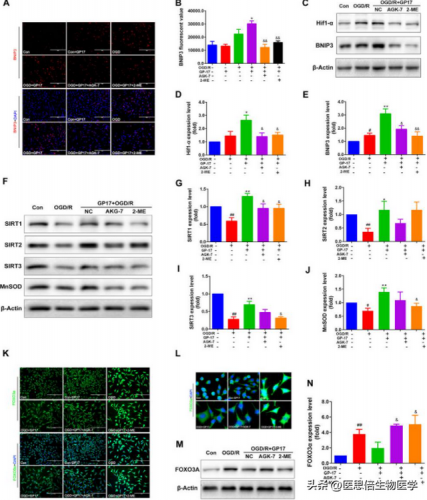
6. 抑制SIRT1/2和Hif1α可消除GP17对OGD/ r致SH-SY5Y细胞中Hif1α- bnip3和SIRT1/2- foxo3a信号通路的影响
GP17 通过激活 Hif1α 和/或 SIRT1/2 信号通路调控线粒体自噬。通过免疫荧光和WB研究 GP17 对Hif1α-BNIP3 和 SIRT1/2-FOXO3A 通路的调控作用,并通过抑制剂 AGK-7 和 2-ME 验证其可能的机制。免疫荧光分析显示,与单纯 OGD/R 作用的 SH-SY5Y 细胞相比,GP17 在 OGD/R 作用的 SH-SY5Y 细胞中的表达显著增加。然而,AGK-7 和 2-ME 预处理逆转了 BNIP3 的表达变化(图 6A, B)。同样,AGK-7 和 2-ME 均显著抑制了GP17 诱导的 Hif1α 和 BNIP3 蛋白的表达(图 6C-E)。作者还发现,与单纯 OGD/R 作用的 SH-SY5Y 细胞相比,GP17 在 OGD/R 作用的 SH-SY5Y 细胞中显著提高了 SIRT1/2/3 和 MnSOD 的表达。AGK-7 显著抑制了 GP17 诱导的这些蛋白表达的增加(图 6F-J)。
创新性
本研究的创新之处在于发现了GP17通过调节SIRT1-FOX03A/Hif1a-BNIP3介导的线粒体自噬途径来保护线粒休免受缺血性损伤的影响。此外,本文还首次研究了GP17对于缺血性脑损伤的神经保护作用,并揭示了其分子机制。
局限性
研究采用的动物模型和细胞模型可能无法完全模拟人体的缺血性中风情况;
研究样本量较小,需要进一步扩大样本量以提高统计学的可靠性;
研究中未涉及GP17的药代动力学和毒性研究。